Christophe Delavaud
1, Julien Lincot
1, Marie-Pierre Debray
1, Élisabeth Schouman-Claeys
1,2, Benjamin Dallaudière
1,21) Service de Radiologie - Imagerie médicale, Hôpital Universitaire Bichat - Claude Bernard, Assistance Publique - Hôpitaux de Paris, 75018 Paris
2) Université Paris Diderot, Faculté de Médecine Xavier Bichat, 75018 Paris
Correspondance : C. Delavaud
E-mail :
christophe.delavaud@hotmail.frObservationUn homme âgé de 70 ans a bénéficié d’une TDM et d’une IRM thoraciques sans injection de produit de contraste (Figures 1 et 2) pour exploration d’un élargissement médiastinal de découverte fortuite sur une radiographie systématique réalisée pour bronchopneumopathie chronique obstructive (BPCO). Le patient était asymptomatique et la BPCO était sa seule pathologie connue. Les examens biologiques étaient normaux.
Fig. 1 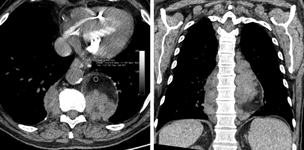
Fig. 1. Scanner thoracique sans injection de produit de contraste iodé en coupes axiale et coronale.
Fig. 2 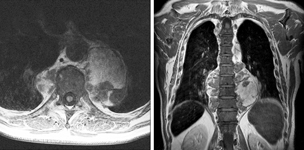
Fig. 2. IRM thoracique en coupe axiale pondérée T1 et en coupe coronale pondérée T2.
Après lecture du cas, quel diagnostic choisiriez-vous parmi les propositions suivantes :
A. Neurinome ;
B. Lymphome ;
C. Liposarcome ;
D. Hématopoïèse extramédullaire ;
E. Lipome.
DiagnosticRéponse : D. Hématopoïèse extramédullaire paravertébrale.
DiscussionLes images scanographiques mettaient en évidence une masse paravertébrale bilatérale hétérogène volumineuse, contenant des zones de densité négative, graisseuse (Figure 3, flèche blanche).
Le patient a refusé l’injection intraveineuse de produit de contraste iodé nécessaire à une caractérisation scanographique plus approfondie. Une IRM thoracique sans injection (Figure 4) effectuée à titre complémentaire a mis en évidence cette même masse paravertébrale bilatérale hétérogène, avec prédominance de zones en hyposignal sur les séquences pondérées T1 et T2 (flèches grises) et de zones en hypersignal graisseux sur les images pondérées T1 et T2 (flèches blanches).
Ces aspects étaient caractéristiques d’une hématopoïèse extramédullaire paravertébrale.
Les corps vertébraux thoraciques montraient un hyposignal global en T1, évocateur d’une moelle régénérative non spécifique. En outre, le foie présentait également une hypointensité globale sur les images pondérées T2, faisant rechercher une surcharge ferrique mais qui n’était pas retrouvé sur le bilan biologique.
Ce patient totalement asymptomatique n’avait aucune affection hématologique connue (en particulier aucune anémie chronique ou pancytopénie) et n’était pas sous chimiothérapie. La myélofibrose pouvait aussi être discutée du fait de la haute densité osseuse au scanner, mais il n’y avait aucun argument biologique en ce sens. La découverte de cette masse a été considérée comme fortuite et aucun traitement n’a été instauré du fait de l’absence de symptomatologie.
L’hématopoïèse extramédullaire (HEM) est secondaire à une pathologie hématologique engendrant une anémie chronique ; le développement du tissu hématopoïétique s’effectue alors en dehors de la moelle osseuse. L’HEM survient habituellement dans des sites embryonnaires de prolifération du tissu hématopoïétique, comme la rate ou le foie, qui arrêtent de produire des érythrocytes à la naissance mais conservent cette capacité en cas d’érythropoïèse inefficace [1]. L’HEM peut également se déclencher dans d’autres tissus mous [2]. Le rachis dorsal est la localisation la plus fréquente d’HEM non hépato-splénique [1] mais son mécanisme reste controversé [3].
Cette affection est asymptomatique dans approximativement 80 % des cas [3, 4] mais des symptômes peuvent apparaître du fait de sa localisation, en particulier en cas de compression radiculaire ou médullaire. [5] L’IRM ou l’anatomopathologie peut confirmer le diagnostic. Les coupes histologiques trouvent un tissu hématopoïétique contenant des cellules de lignées érythroïdes et myéloïdes qui sont immatures et matures [6].
À l’IRM, la moelle rouge extramédullaire en régénération a habituellement un aspect de masse nettement délimitée, de signal isointense ou hypointense sur les images pondérées T1 et T2, avec rehaussement minime ou nul après injection de gadolinium. Ces infiltrations hématopoïétiques extramédullaires actives peuvent être associées, au sein de la même masse, à des zones inactives plus anciennes ayant l'aspect d'une infiltration graisseuse en hypersignal sur les séquences pondérées T1 et T2, comme dans le cas que nous présentons [7]. Il est intéressant de noter qu’en cas de maladie hémolytique, un dépôt ferrique hypointense peut également être observé. Contrairement au cas décrit par Guermazy et al. [5], notre cas ne présentait pas d’extension au canal médullaire et la cause sous-jacente n’a pas été identifiée.
Dans notre cas, la présence de ces aspects typiques en IRM a évité une biopsie percutanée, dont les indications se limitent aux contre-indications de l’IRM et aux aspects atypiques en IRM faisant suspecter une prolifération maligne. Le traitement étiologique de l’HEM consiste à traiter l’anémie sous-jacente, notamment par des transfusions sanguines. Aucun traitement n'est nécessaire si l’HEM est asymptomatique. En cas de compression radiculaire ou médullaire, le traitement pourra, selon le cas, consister en une radiothérapie à faible dose ou une exérèse chirurgicale [3].
Fig. 3 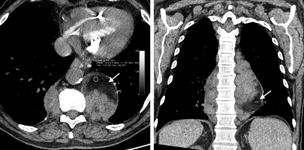 Fig. 3. Scanner thoracique sans injection de produit de contraste iodé en coupes axiale et coronale. Masse paravertébrale bilatérale hétérogène volumineuse contenant une densité négative graisseuse (flèches blanches).
Fig. 4
Fig. 3. Scanner thoracique sans injection de produit de contraste iodé en coupes axiale et coronale. Masse paravertébrale bilatérale hétérogène volumineuse contenant une densité négative graisseuse (flèches blanches).
Fig. 4 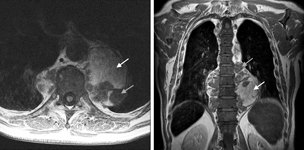
Fig. 4. IRM thoracique en coupe axiale pondérée T1 et en coupe coronale pondérée T2. Même masse paravertébrale bilatérale hétérogène avec zones prédominantes en hyposignal sur les images pondérées T1 et T2 (flèches grises) et zones en hypersignal graisseux sur les images pondérées T1 et T2 (flèches blanches).
Conflits d’intérêts
Aucun.
Références
1. Koch CA, Li CY, Mesa RA, Tefferi A. Nonhepatosplenic extramedullary hematopoiesis: associated diseases, pathology, clinical course, and treatment. Mayo Clin Proc. 2003; 78(10):1223-1233.
2. Rajiah P, Hayashi R, Bauer TW, Sundaram M. Extramedullary hematopoiesis in unusual locations in hematologically compromised and noncompromised patients. Skeletal Radiol. 2011; 40(7):947-953.
3. Haidar R, Mhaidli H, Taher AT. Paraspinal extramedullary hematopoiesis in patients with thalassemia intermedia. Eur Spine J. 2010; 19(6):871-878.
4. Parsa K, Oreizy A. Nonsurgical approach to paraparesis due to extramedullary hematopoiesis. Report of two cases. J Neurosurg. 1995; 82(4):657-660.
5. A. Guermazi, E. de Kerviler, D. Cazals-Hatem, A.-M. Zagdanski, J. Frija Imaging findings in patients with myelofibrosis. Eur Radiol 1999;9(7):1366-75.
6. Tsitouridis J, Stamos S, Hassapopoulou E, Tsitouridis K, Nikolopoulos P. Extramedullary paraspinal hematopoiesis in thalassemia: CT and MRI evaluation. Eur J Radiol. 1999; 30(1):33-38.
7. Yamato M, Fuhrman CR. Computed tomography of fatty replacement in extramedullary hematopoiesis. J Comput Assist Tomogr. 1987; 11(3):541-542.

